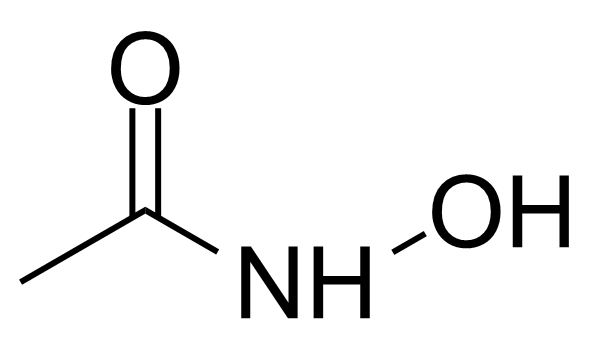
Acetohydroxamic acid
Ce produit n’est plus fabriqué, mais il nous reste encore un peu de stock.
N-hydroxyacetamide
Pour plus d’informations ou si vous avez des questions, veuillez nous envoyer un e-mail georganics@georganics.sk ou utiliser notre formulaire de contact
Informations réglementaires

H302 – Nocif en cas d’ingestion.
H312 – Nocif par contact cutané.
H315 – Provoque une irritation cutanée.
H319 – Provoque une sévère irritation des yeux.
H332 – Nocif par inhalation.
H335 – Peut irriter les voies respiratoires.
P261 – Éviter de respirer les poussières/fumées/gaz/brouillards/vapeurs/aérosols.
P280 – Porter des gants de protection/des vêtements de protection/un équipement de protection des yeux/du visage.
P301+312 – EN CAS D’INGESTION: appeler un CENTRE ANTIPOISON ou un médecin en cas de malaise.
P302+352 – EN CAS DE CONTACT AVEC LA PEAU: laver abondamment à l’eau et au savon.
P305+351+338 – EN CAS DE CONTACT AVEC LES YEUX: rincer avec précaution à l’eau pendant plusieurs minutes. Enlever les lentilles de contact si la victime en porte et si elles peuvent être facilement enlevées. Continuer à rincer.
Catégorisation des produits
Description
Acetohydroxamic acid est un composé chimique utile avec une variété d'utilisations de recherche. Nous sommes heureux d'offrir des Acetohydroxamic acid de haute qualité dans différentes tailles (pour la recherche, l’échelle pilote ou les applications de production) du milligramme aux lots de plusieurs kilogrammes, ce qui vous permet de sélectionner facilement la bonne quantité pour vos besoins.
Afficher la description complèteGeneral description of Acetohydroxamic acid:
Acetohydroxamic acid (AHA) [546-88-3] also known under trade names Lithostat (US) or Uronefrex (EU) is a compound, structurally similar to urea. In a pure form, it is a white crystalline solid with melting point of 90-91 °C.[1] The structure of the hydroxamic acids was first brought to the attention by W. Lossen in 1869.[2] Few years later he observed, apparently by accident, that thermal decomposition of hydroxamic acid led to the isocyanate. This reaction was later named after him as Lossen rearrangement.[3] The most general method of preparation is the reaction between ethylacetate or acetic anhydride and hydroxylamine in absolute alcohol. The reaction proceeds rapidly at room temperature, particularly in the presence of an equimolecular quantity of sodium alkoxide.[4] Alternatively, AHA can be prepared from acetyl chloride and hydroxylamine with sodium carbonate in ether/water.[5]Application of Acetohydroxamic acid:
Acetohydroxamic acid is a potent urease inhibitor of bacterial urease activity, especially Helicobacter pylori.[6] It was found to be useful in treating urinary tract infections by preventing urine alkalization. Although this compound had severe side effects, such as teratogenicity, psychoneurologic and musculo-integumentary symptoms, it was approved by the FDA in 1983 to treat chronic urea-splitting urinary infections.[7] It is used, in addition to antibiotics or medical procedures, to treat chronic urea-splitting urinary infections. It can be oxidized in situ to nitrosocarbonylmethane which reacts in Diels–Alder reaction with 1,3-dienes.[5] Acetohydroxamic acid is a good chelating agent for heavy metals[8] such as copper, iron, cobalt, nickel, chromium, manganese, uranium. It has been suggested as a partitioning agent for the separation of uranium and plutonium in nuclear fuel reprocessing.[9]Product categorization (Chemical groups):
Main category: Second level: ______________________________________________________________________________________Produits similaires
| Nom du produit | Structure | Numéro CAS | G-code | |
|---|---|---|---|---|
| Acetohydroxamic acid |  | [546-88-3] | GEO-00010 | |
| 1-Adamantanecarboxylic acid | 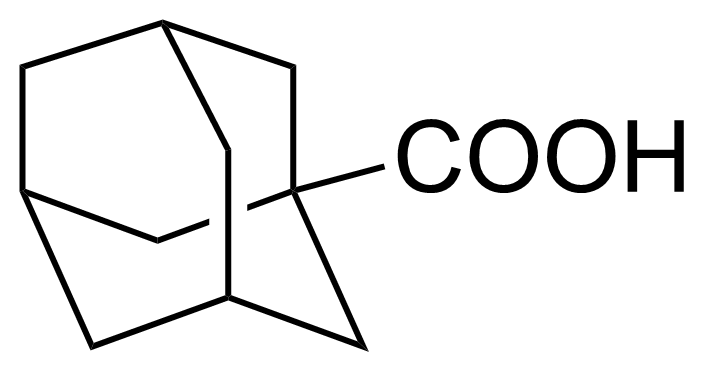 | [828-51-3] | GEO-04336 | |
| Nouveau | 4-Amino-5-nitrophthalic acid | 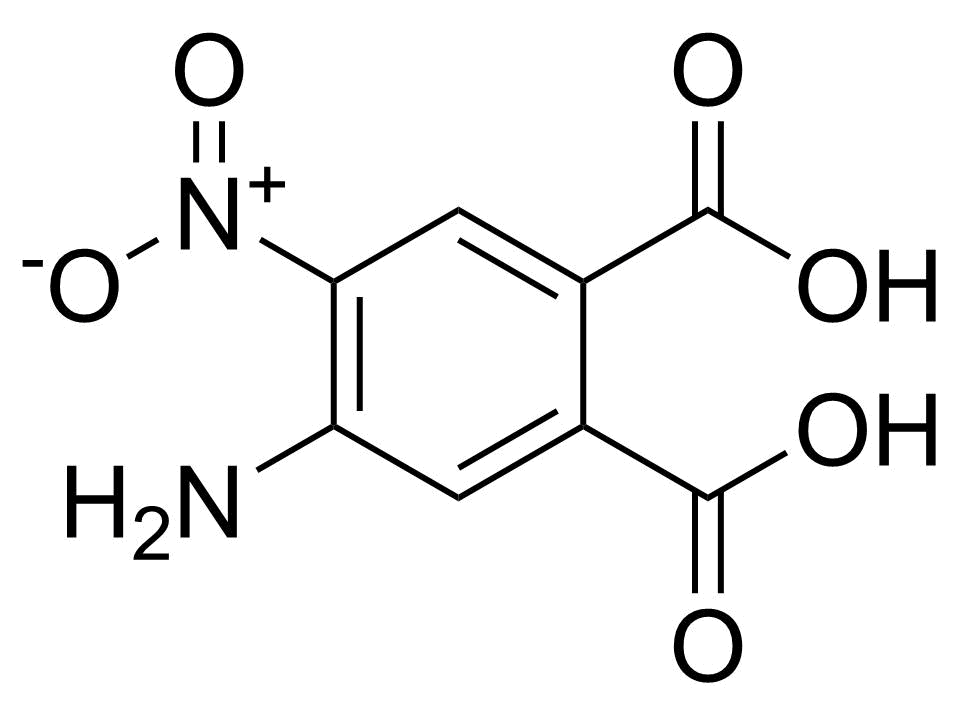 | [89939-49-1] | GEO-04810 |
| 3H-1,2-Benzodithiol-3-one 1,1-dioxide | 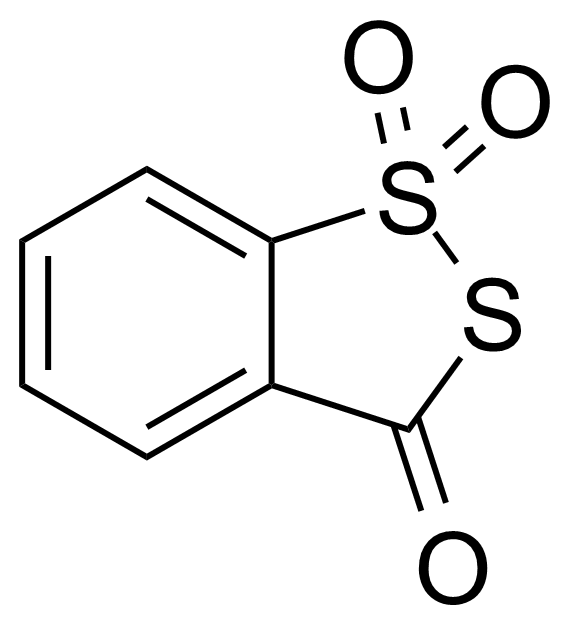 | [66304-01-6] | GEO-04361 | |
| Benzo[b]thiophene-2-carboxylic hydrazide | ![Structure of Benzo[b]thiophene-2-carboxylic hydrazide](https://georganics.sk/wp-content/uploads/2021/05/GEO-00294_Benzobthiophene-2-carboxylic_hydrazide.png) | [175135-07-6] | GEO-00294 | |
| N-Benzylmaleimide dihydrate | 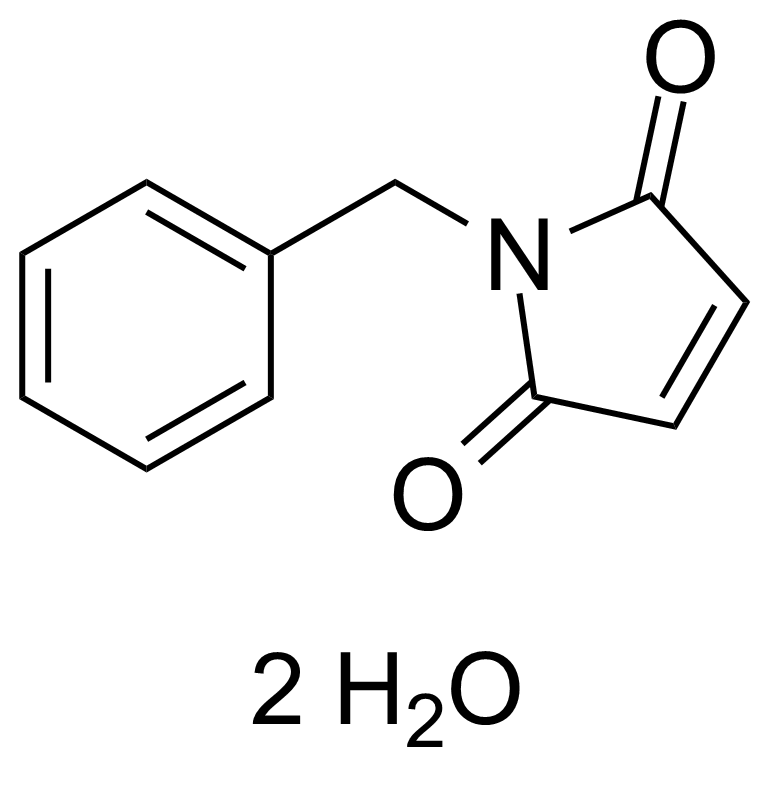 | [1631-26-1] | GEO-00303 | |
| Bromoacetic acid anhydride | 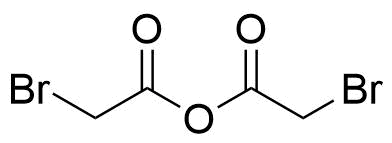 | [13094-51-4] | GEO-04577 | |
| 2-(6-Bromohexyl)isoindoline-1,3-dione | 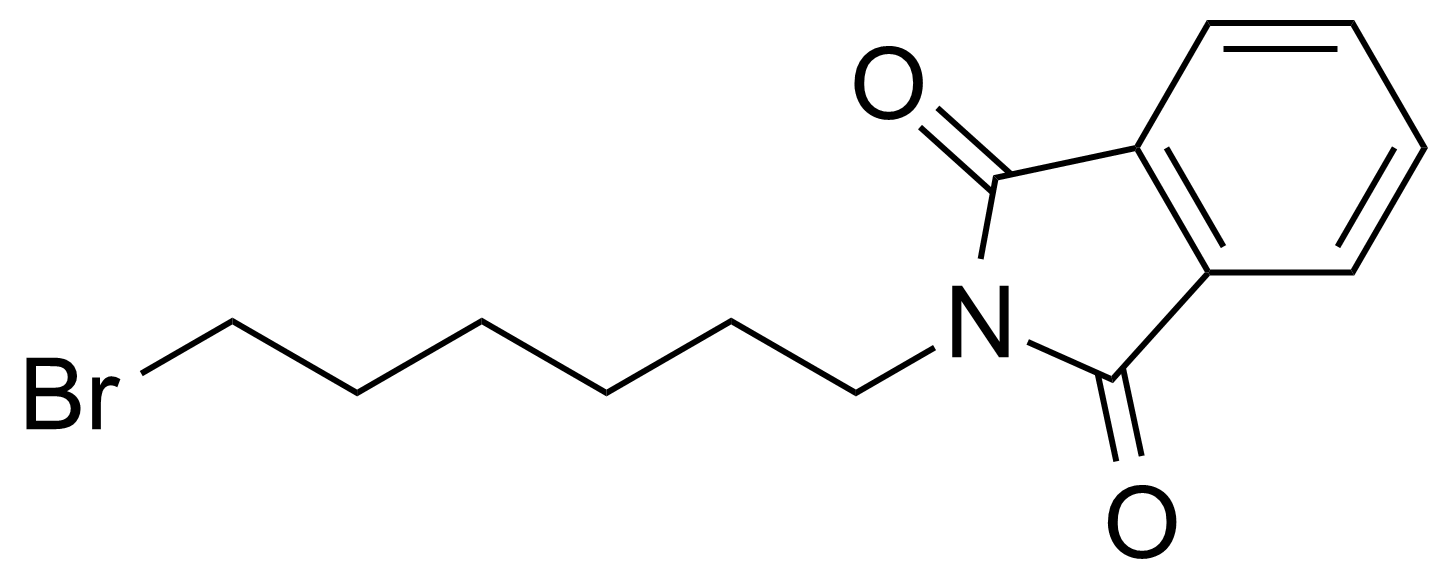 | [24566-79-8] | GEO-04399 | |
| Nouveau | 7-Bromoisoquinoline-4-carboxylic acid | 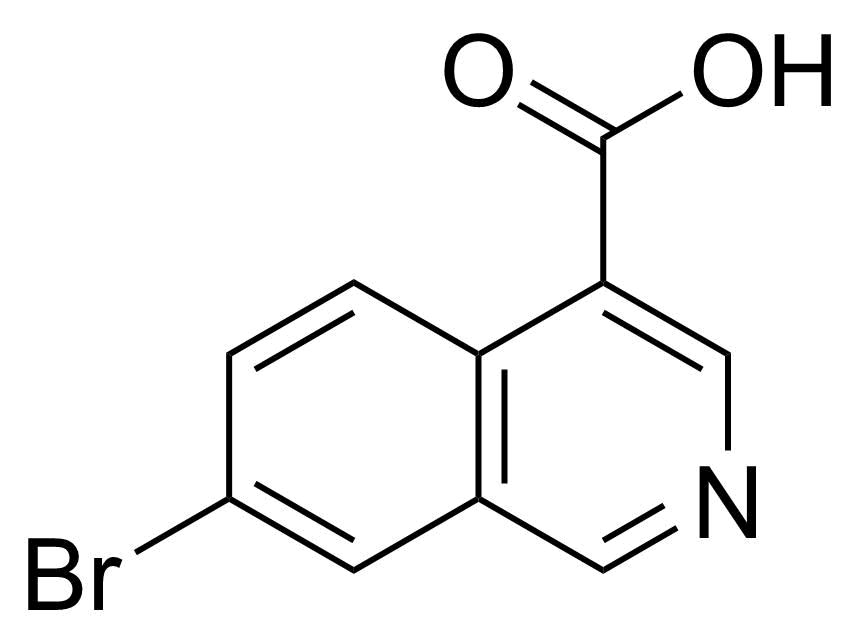 | [31009-04-8] | GEO-04828 |
| Bromomaleic anhydride | 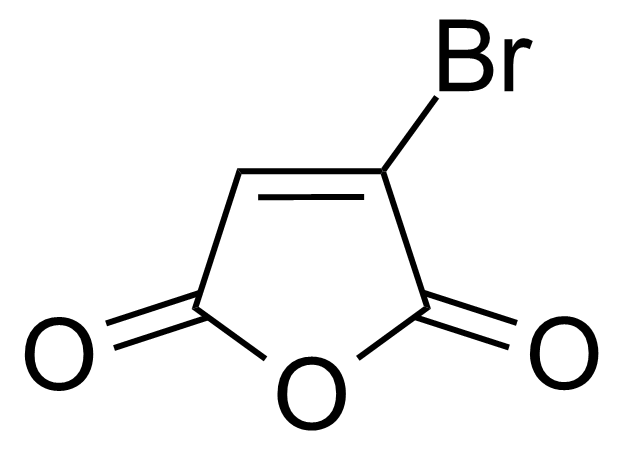 | [5926-51-2] | GEO-00484 |